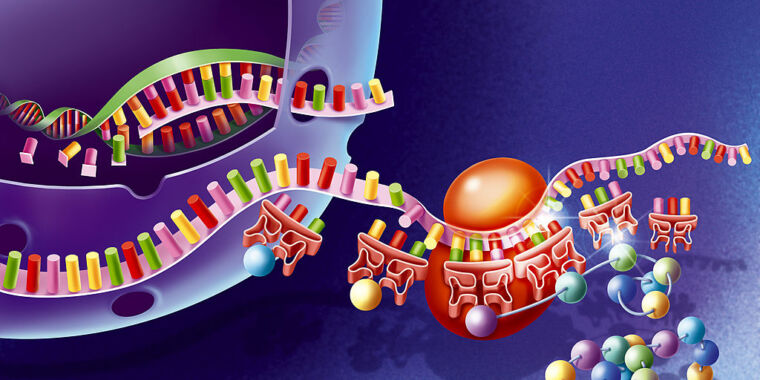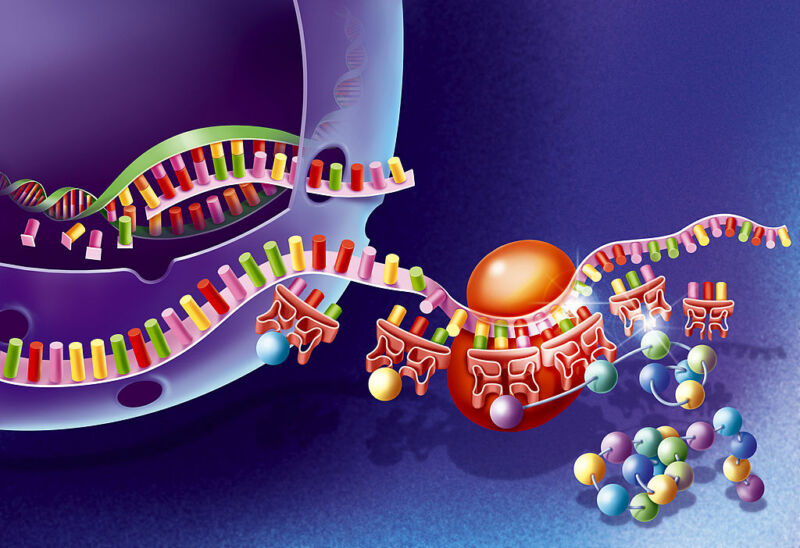
Alle Lebewesen auf der Erde verwenden eine Version des gleichen genetischen Codes. Jede Zelle stellt Proteine mit den gleichen 20 Aminosäuren her. Ribosomen, die Maschinerie zur Herstellung von Proteinen in Zellen, lesen den genetischen Code von einem Boten-RNA-Molekül, um zu bestimmen, welche Aminosäure neben dem spezifischen Protein, das sie aufbauen, hinzugefügt werden soll.
Dieser Code ist universell, weshalb die Ribosomen in unseren Zellen ein Stück viraler Boten-RNA lesen und in ein funktionsfähiges virales Protein verwandeln können. Es gibt jedoch noch viele andere Aminosäuren. Obwohl das Leben sie im Allgemeinen nicht verwendet, haben Wissenschaftler sie in Proteine eingebaut. Jetzt haben Forscher einen Weg gefunden, den genetischen Code enorm zu erweitern und eine weit verbreitete Aufnahme dieser nicht-biologischen Aminosäuren zu ermöglichen. Sie erreichen dies, indem sie einen zweiten Satz von allem ausführen – Proteine und RNAs –, die für die Übersetzung des genetischen Codes erforderlich sind.
Ein System für sich
Nicht-kanonische Aminosäuren können eine Reihe von Funktionen erfüllen. Sie können als Markierungen fungieren und es einfacher machen, das spezifische Protein eines Forschers in Zellen zu verfolgen. Sie können helfen, die Funktion eines Proteins zu regulieren, sodass Forscher es zu einem bestimmten Zeitpunkt und Ort ihrer Wahl aktivieren und deaktivieren und dann seine nachgelagerten Wirkungen beobachten können. Wenn genügend dieser nicht-kanonischen Aminosäuren aneinandergereiht würden, würden die resultierenden Proteine eine völlig neue Klasse von Biopolymeren bilden, die Funktionen erfüllen könnten, die herkömmliche Proteine nicht erfüllen können – für Forschungs-, Therapie- oder andere Zwecke.
Um nicht-kanonische Aminosäuren in Proteine einzubauen, muss man am genetischen Code basteln, der für seine Verwendung in keiner Weise spezifiziert werden kann. Eine Möglichkeit ist zu den genetischen Code der Zelle bearbeiten, so dass das meiste davon intakt bleibt. Eine Alternative verwendet modifizierte Versionen aller Komponenten des genetischen Codes: orthogonale mRNAs, orthogonale Ribosomen und orthogonale Enzyme, die für das Lesen der mRNAs und den Aufbau der Proteine in den Ribosomen verantwortlich sind. Orthogonal bedeutet hier, dass diese Maschinerie neben der normalen ribosomalen Proteinherstellungsmaschinerie in einer Zelle läuft, sie aber nicht stört. Es liest und übersetzt nur seine eigenen orthogonalen mRNAs, nicht die normalen zellulären.
Diese orthogonalen Komponenten wären fremd, also für das Funktionieren der Zelle nicht wesentlich. Sie können daher unterschiedlich gestaltet und reguliert und beliebig modifiziert werden. Sie können verwendet werden, um neue Polymere herzustellen und die Mechanismen der normalen zellulären Proteinproduktion aufzuklären. Das können wir mit den normalen Zellbestandteilen nicht machen, denn das würde die Zelle töten.
Orthogonalität optimieren
Jason chin, Leiter des Centre for Chemical & Synthetic Biology (CCSB) in Cambridge, UK, hat all diese orthogonalen Komponenten geschaffen. Aber sie sind nicht sehr effizient. In einem diese Woche veröffentlichten Artikel in Natürliche Chemie, beschreibt er, wie er das gelöst hat: indem er Computeralgorithmen verwendet, um automatisch zu entwerfen und zu optimieren, welche orthogonalen mRNAs am besten von orthogonalen Ribosomen übersetzt werden. Er verbesserte nicht nur die Proteinausbeute drastisch, sondern bewirkte auch, dass orthogonale Ribosomen effizient arbeiteten, selbst wenn normale Ribosomen vorhanden waren.
„Unser Verständnis der Faktoren, die die Proteinausbeute für die natürliche Translation bestimmen, ist unvollständig … nur die Hälfte der Varianz der beobachteten Proteinausbeute kann durch bekannte Parameter erklärt werden“, bedauert die Präambel der Arbeit. Trotzdem wusste sein Labor, dass der Initiationsschritt, wenn das Ribosom die Boten-RNA greift, ein wichtiger Schritt ist. Sie wussten auch, dass die Struktur der mRNA wichtig ist. Also begannen sie, ihre orthogonale mRNA zu mutieren, um diese beiden Aspekte zu ändern, und wählten die Mutanten aus, die orthogonale Ribosomen gut binden, aber normale Ribosomen weniger gut. Nach Hunderten von Mutationsrunden hatten sie drei verschiedene orthogonale mRNAs optimiert, die für drei verschiedene Proteine kodieren. Einer enthielt vier nicht-kanonische Aminosäuren.
Das Labor wandte dann den gleichen Ansatz zur Optimierung orthogonaler Enzyme an und erzielte eine 33-fache Steigerung der Proteinausbeute; das orthogonale System produzierte jetzt genauso viel Protein wie das normale zelluläre System. Die in dieser Arbeit verwendeten Zellen waren: E coli, aber Dr. Chin hat ein orthogonales System verwendet, um nicht-kanonische Proteine in Hefe, Säugerzellen, Würmern und Fruchtfliegen herzustellen.
„Wir gehen davon aus, dass die Möglichkeiten, die sich aus Ansätzen ergeben, mehrere verschiedene nicht-kanonische Aminosäuren einzubauen, mit zunehmender Anzahl verschiedener nicht-kanonischer Aminosäuren, die eingebaut werden können, zunehmen werden“, schreiben er und seine Kollegen. Diese von ihnen entwickelten Algorithmen zum effizienten Design translatierter orthogonaler mRNAs sollten ihnen sicherlich dabei helfen, dieses Ziel zu erreichen.
natürliche Chemie, 2021. DOI: 10.1038/s41557-021-00764-5